南湖网讯(通讯员 裴凯)2018 年6月21日,国际知名学术期刊《Nucleic Acids Research》在线发表了我校生科院/作物遗传改良国家重点实验室殷平教授团队关于DapF-RppH复合物结构和功能的最新研究进展,论文以“DapF stabilizes the substrate-favoring conformation of RppH tostimulate its RNA-pyrophosphohydrolase activity in Escherichia coli” 为题,报道了第一个RNA的5′端三磷酸基团水解复合物的结构,并阐明了DapF蛋白调节RppH活性的分子机制。
mRNA的迅速降解是细胞适应环境的一种生存策略,其5′端状态是mRNA被降解速率的决定因素之一。mRNA的5′端常携有一类“帽子”结构,如m7G及其衍生物、NAD和三磷酸基团,它们能帮助mRNA抵抗来自各种核酸内切酶和外切酶的降解;只有当这些“帽子”结构被特定的水解酶去除以后,mRNA才能被核酸酶进一步降解。细胞体内有一系列的“去帽”酶,如Dcp2、NudC和RppH等,负责"帽子”结构的水解。这一类“去帽”酶的活性受调节,它们能与各种辅因子形成“去帽”复合物,加速对“帽子”结构的水解速率,研究这些“去帽”酶与其底物、其调控因子复合物的结构和功能可加深我们对胞内RNA降解调控的理解。
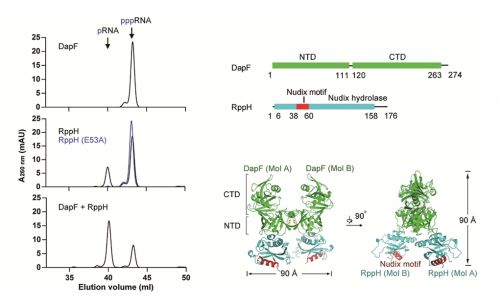
RppH是一种焦磷酸水解酶,在细菌当中广泛存在,它能水解mRNA的5′端三磷酸基团,其活性受到辅因子DapF蛋白的直接调控。在DapF蛋白存在下,RppH能加速目标mRNA的降解,但是其分子机制不清楚。在殷平教授课题组的这项研究当中,他们解析了DapF和RppH蛋白复合物的高分辨率晶体结构(2.3 Å),并且通过一系列生化分析和结构比对,发现DapF与RppH结合后,促进了后者发生轻微的构象变化,从而增强了RppH与底物RNA的结合。这些实验结果清晰的解释了DapF蛋白促进RppH活性的分子机制,为进一步寻找细菌中“去帽”复合物的新成员奠定了良好的基础。该研究不仅回答了细菌体内mRNA降解的几个关键科学问题,并且为针对致病菌的药物开发能提供新的潜在作用靶点。
据悉,此篇文章是殷平教授课题组关于RNA代谢调控研究的系列工作之一,2016年8月,其课题组关于RNA的5′端NAD修饰降解的工作就以题为“Structuralbasis of prokaryotic NAD-RNA decapping by NudC”的论文发表在《Cell Research》杂志上,这两个相关的工作利用结构生物学和生物化学的方法,阐述了关于RNA的5′端保护结构是如何被水解以及如何被调控,从而影响RNA的代谢。
我校生科院博士生王强和副研究员张德林为该论文共同第一作者,殷平教授为通讯作者。该研究工作获得了华中农业大学自主科技创新基金和人才启动基金的经费资助,我校蛋白质平台为该研究提供了强有力的支持,上海同步辐射光源BL17U1和国家蛋白质科学中心BL19U1线站为晶体衍射数据收集提供了必要保障。
文章链接:
https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gky528/5042035
https://www.nature.com/articles/cr201698
审核人:殷平


已有0人发表了评论