南湖新闻网讯(通讯员 李冰雪)近日,我校资源与环境学院、动科动医学院、生物医学与健康学院与中国科学院武汉病毒研究所联合攻关,在广谱抗SARS-CoV-2药物——基于水凝胶聚合物纳米颗粒的非生物合成抗体抑制剂研究方面取得重要进展。该研究成果以“Abiotic Synthetic Antibody Inhibitor with Broad-Spectrum Neutralization and Antiviral Efficacy against Escaping SARS-CoV-2 Variants”为题在线发表在纳米科技领域学术期刊ACS Nano上。
SARS-CoV-2的大流行以及人们对其“特效药”的迫切需求,使得抗病毒药物研究得到快速发展。以SARS-CoV-2刺突蛋白(S蛋白)为成药靶点研发的中和抗体是目前已知预防和抑制SARS-CoV-2感染最有效的候选药物之一。然而抗SARS-CoV-2抗体药物在研发和应用过程中存在许多局限性,包括开发和生产成本高、耗时长、稳定性和稳健性差、保质期短、具有潜在免疫原性以及对SARS-CoV-2突变株中和作用减弱甚至失效等。随着SARS-CoV-2变异株的不断迭代,免疫逃逸或抗体突破感染病例层出不穷,生物抗体药物的某些弊端已无法被忽视。水凝胶聚合物纳米颗粒因其稳定性高、粒径小且可控、毒性低、生物相容性好以及可设计性,在生物毒素以及病原菌蛋白的吸附螯合、分离纯化、分析检测、临床诊断和靶向治疗等方面的成功应用引起极大关注。开发基于水凝胶聚合物纳米颗粒的非生物合成抗体抑制剂有望克服生物抗体的诸多不足而成为一种广谱型抗SARS-CoV-2靶向治疗药物。
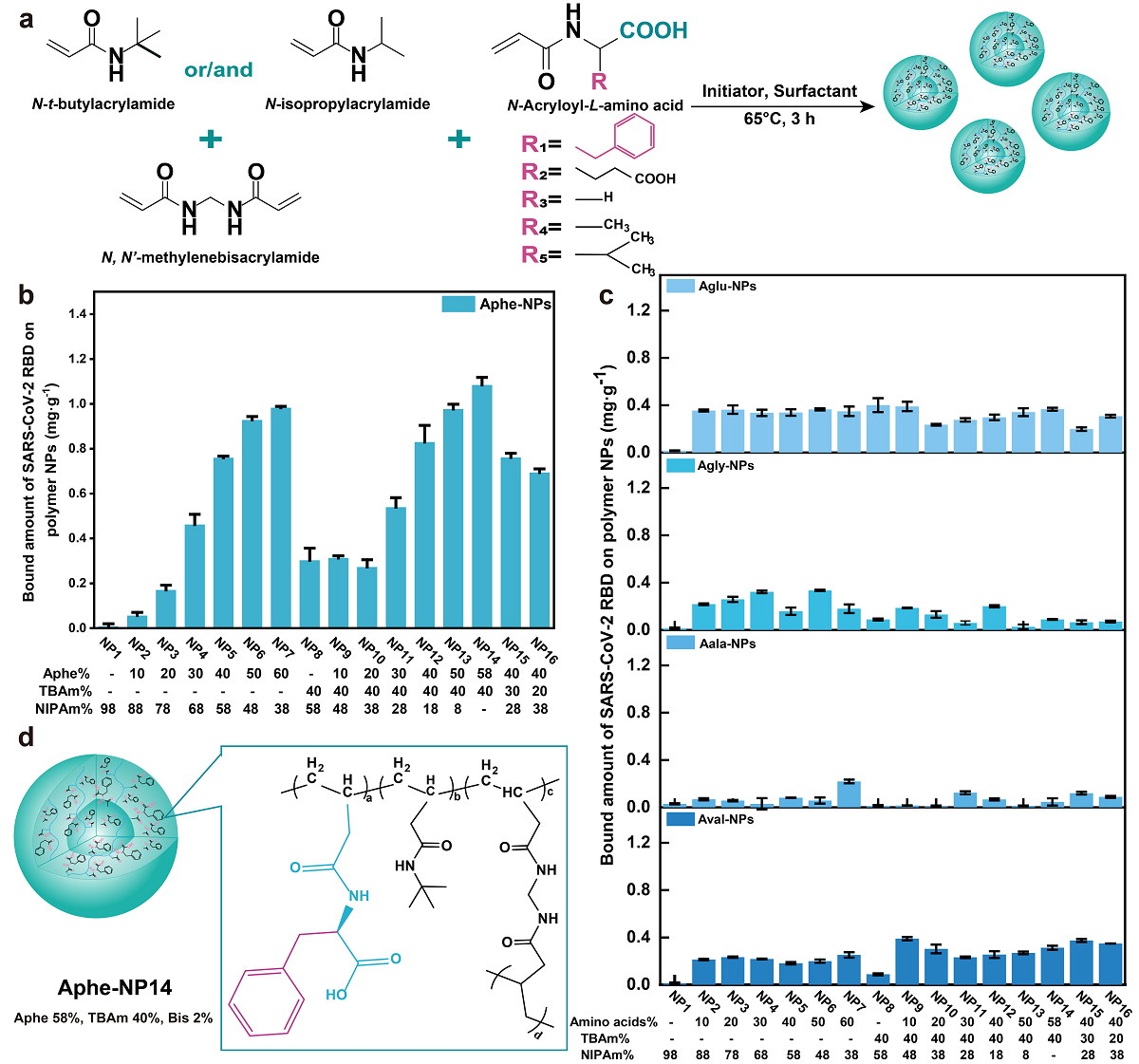
水凝胶聚合物纳米颗粒文库的制备及与SARS-CoV-2 S蛋白RBD的亲和筛选
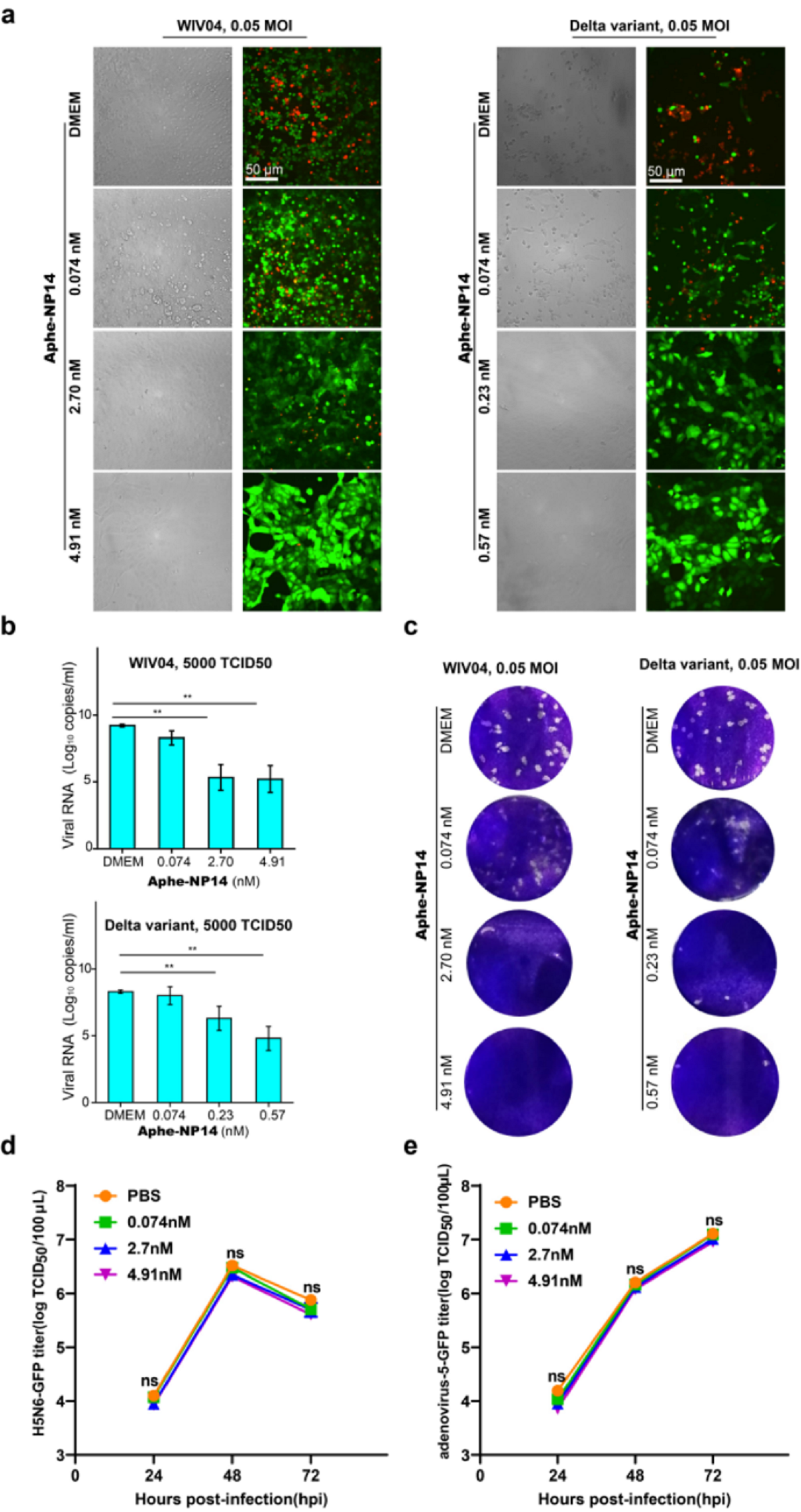
Aphe-NP14对SARS-CoV-2感染Vero E6细胞的抑制作用
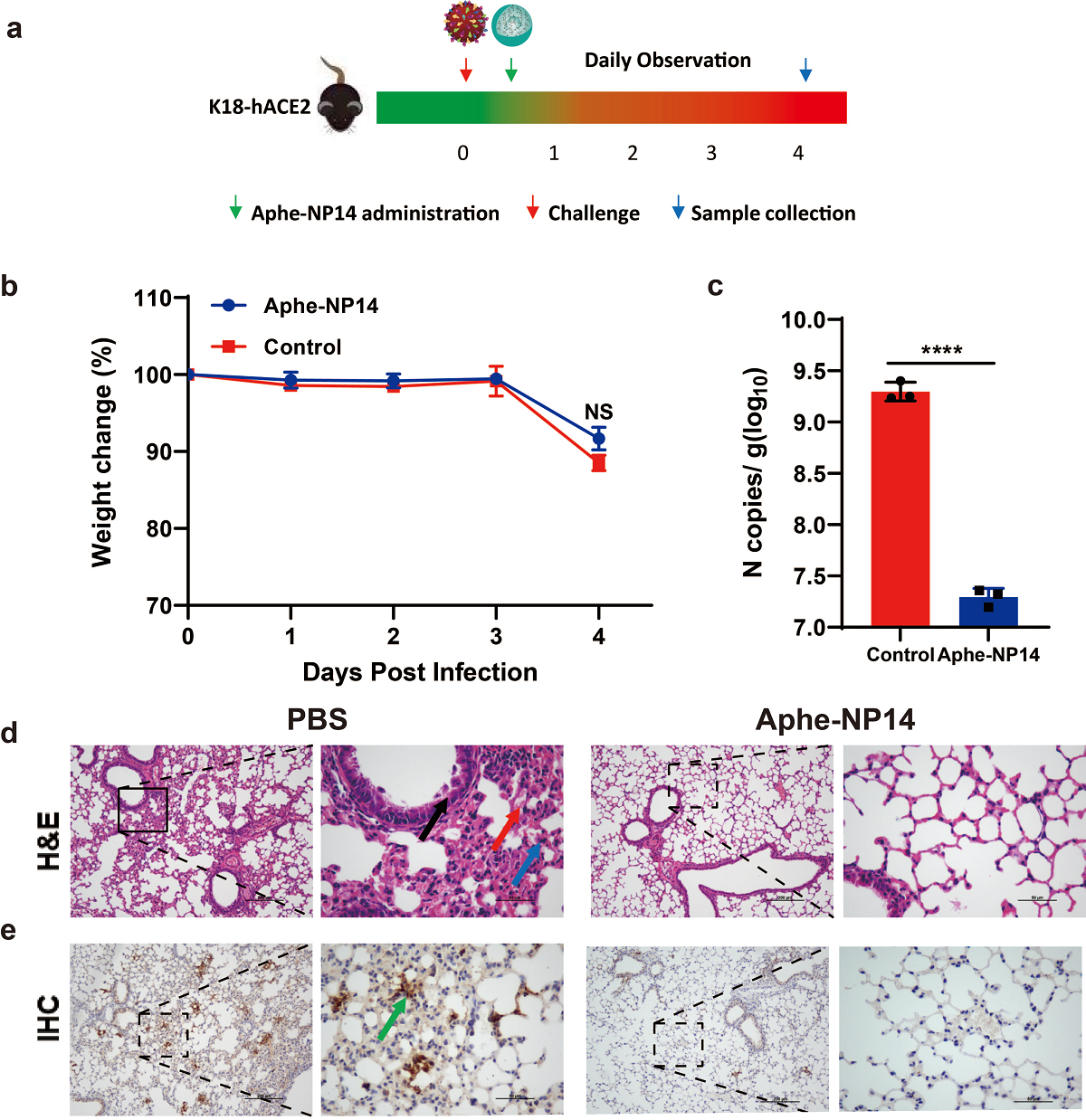
Aphe-NP14对 SARS-CoV-2感染K18-hACE2转基因小鼠的体内抑制作用
该研究报道了一种非生物合成抗体抑制剂研发策略。该策略以S蛋白RBD─ACE2(血管紧张素转换酶2)复合物的晶体结构和分子识别机制为指导,采用理性设计选择与S蛋白RBD关键残基互补的具有芳香和负电荷基团的N-丙烯酰基-L-苯丙氨酸(Aphe)为候选功能单体,调节功能和共存单体的种类和配比构建出一个容量更小、靶向性更强的水凝胶聚合物纳米颗粒文库,通过亲和筛选从中定向进化出一种对SARS-CoV-2 S蛋白RBD突变体具有高亲和性和广谱选择性的聚合物纳米颗粒Aphe-NP14。利用该策略不仅可以减轻合成任务,缩短抑制剂开发时间,还可以使筛选得到的非生物合成抗体抑制剂具有更强的靶向治疗作用。研究结果表明,筛选的APhe-NP14对野生型和当前的主要关切变异株(Beta、Delta和Omicron)S蛋白 RBD具有高吸附容量、快速吸附动力学、强亲和力以及在生物相关条件下的广泛特异性。体外实验表明,Aphe-NP14与S蛋白RBD的特异亲和使其对不同S蛋白突变体包装的假病毒颗粒以及SARS-CoV-2病毒突变株具有高效中和作用,因此可以阻断其与细胞受体表面ACE2的结合,进而抑制病毒对宿主细胞的入侵及在细胞体内的复制和增殖。对感染SARS-CoV-2病毒的K18-hACE2转基因小鼠实施鼻内给药治疗方案,结果发现与对照组相比,小鼠肺部病毒RNA和病毒抗原显著降低,由病毒感染引起的肺部损伤也得到明显改善。由此可见,Aphe-NP14在生物体内依然对SARS-CoV-2感染具有强的抑制和治疗作用。此外,在Aphe-NP14用药浓度等于甚至大于有效剂量时,在细胞和小鼠体内均没有观察到明显的毒性效应,表明该抑制剂具有良好的生物相容性和用药安全性。
综上所述,该研究开发的非生物合成抗体抑制剂Aphe-NP14在预防和治疗SARS-CoV-2变异株感染方面具有潜在应用价值,未来可能成为一种潜在的高效、经济和广谱型抗SARS-CoV-2候选药物。该研究工作也为进一步开发靶向SARS-CoV-2其它结构和非结构蛋白,包括核衣壳蛋白、主蛋白酶和RNA依赖性RNA聚合酶的非生物合成抗体抑制剂提供了借鉴。
我校资源与环境学院博士研究生李冰雪和动科动医学院博士研究生赵亚为论文共同第一作者,资源与环境学院刘名茗教授、生物医学与健康学院张强副教授、中国科学院武汉病毒研究所李炜副研究员和我校动科动医学院金梅林教授为论文共同通讯作者。我校资源与环境学院谭文峰教授参与了本项研究并给予了大力支持。该研究工作得到国家自然科学基金、中央高校基本科研业务费专项资金、湖北省科技重大专项和教育部新世纪优秀人才支持计划的资助。
审核人:刘名茗 张强 金梅林
【英文摘要】
The rapid emergence and spread of vaccine/antibody-escaping variants of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) has posed serious challenges to our efforts in combating corona virus disease 2019 (COVID-19) pandemic. A potent and broad-spectrum neutralizing reagent against these escaping mutants is extremely important for the development of strategies for the prevention and treatment of SARS-CoV-2 infection. We herein report an abiotic synthetic antibody inhibitor as a potential anti-SARS-CoV-2 therapeutic agent. The inhibitor, Aphe-NP14, was selected from a synthetic hydrogel polymer nanoparticle library created by incorporating monomers with functionalities complementary to key residues of the SARS-CoV-2 spike glycoprotein receptor binding domain (RBD) involved in human angiotensin-converting enzyme 2 (ACE2) binding. It has high capacity, fast adsorption kinetics, strong affinity, and broad specificity in biologically relevant conditions to both the wild type and the current variants of concern, including Beta, Delta, and Omicron spike RBD. The Aphe-NP14 uptake of spike RBD results in strong blockage of spike RBD–ACE2 interaction and thus potent neutralization efficacy against these escaping spike protein variant pseudotyped viruses. It also inhibits live SARS-CoV-2 virus recognition, entry, replication, and infection in vitro and in vivo. The Aphe-NP14 intranasal administration is found to be safe due to its low in vitro and in vivo toxicity. These results establish a potential application of abiotic synthetic antibody inhibitors in the prevention and treatment of the infection of emerging or possibly future SARS-CoV-2 variants.
